- 製品
- 製品
- CrossLab サポート商品
- サポート商品
- テクニカルサポート
- HOME
- メールニュースアーカイブ
- Access Agilent メールサンプル
- Access Agilent 2010年7月号 記事一覧
- モノクローナル抗体の完全な特性分析を実現する Agilent HPLC-Chip/Q-TOF
>> Access Agilent 購読ご希望の方はこちらからご登録ください | 7月号記事一覧
モノクローナル抗体の完全な特性分析を実現する
Agilent HPLC-Chip/Q-TOF
Keith Waddell
アジレント LC/MS アプリケーションソリューションマネージャ
Ravindra Gudihal
アジレント アプリケーションサイエンティスト
mAb の特性分析に欠かせない LC/MS
質量分析 (MS) は、mAb の構造分析に欠かせません。MS では、インタクトタンパク質の質量、アミノ酸配列、ジスルフィド結合、修飾糖の構造およびプロファイル、さまざまな翻訳後修飾および生成後修飾など、多くの構造特性を測定することができます。このことを示すために、Agilent HPLC-Chip/Q-TOF システムを用いて、市販されている mAb を分析しました。
 | |
| |
 | |
| |
 | |
|
複数の形態を特定するインタクトタンパク質分析
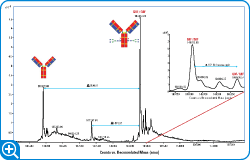
アジレントのシステムを使えば、きわめて少量のインタクト mAb サンプルを確実に分析することができます。エレクトロスプレー精密質量スペクトルを生成し、異型を検出することが可能です。この分析例では、多価チャージスペクトルのデコンボリューションにより、mAb 複合体の 3 つの主要異型 (図 1) が、以下の質量ピークとともに検出されました。
図 1 の挿入図で G1F と示されている、148974.97 Da におけるもう 1 つのピークは、抗体の G0F グリカン部に付加されたヘキソース部と推測されました。観察された質量増加値は 162.16 Da で、計算上の質量増加値 162.14 Da とほぼ一致しています。
質量 145922.00 Da における非グリコシル化種の質量ピーク割り当てを確認するために、mAb を酵素により脱グリコシル化し、分析しました。また、ジチオスレイトール (DTT) を用いて mAb を完全還元し、軽鎖と重鎖の分断により構造をさらに分析しました。LCGC の論文では、これらの分析の結果が説明されています。いずれの実験でも、必要なサンプル量はナノグラムレベルという少ないものでした。
配列を確認するペプチドマッピング
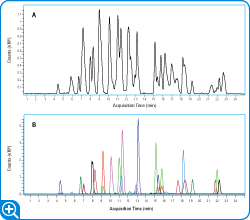
LC/MS を用いたペプチドマッピングは、アミノ酸配列や修飾位置の確認および同定の分析ツールとして確立されています。トリプシン消化後、mAb を分析して得られたペプチドピークのベースピーククロマトグラム (BPC) を図 2A に示しています。重鎖および軽鎖を構成するペプチドの抽出イオンクロマトグラム (EIC) は、Agilent HPLC-Chip/Q-TOF システムにより得られる優れたクロマトグラフィ分離能を示しています (図 2B)。
この分析によりマッチしたペプチドは、重鎖の 95 %、軽鎖の 85 % を占めています。しかし、mAb の特性分析および品質管理では、すべてのアミノ酸を特定する必要があります。この要件を満たすために、さらに 2 つのプロテアーゼ (黄色ブドウ球菌由来の Glu-C、およびキモトリプシン) を使用しました。これらを用いた消化により得られたデータ (ここには示さず) は、トリプシン消化のみでは検出されなかった配列をカバーしています。
グリコシル化領域を特定する MS および MS/MS 分析
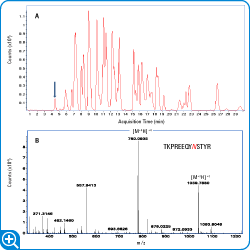
mAb のトリプシン消化物の HPLC-Chip/Q-TOF 分析では、グリコペプチドが 4.42 分で溶出しました (図 3A)。図 3B にスペクトルを示しています。グリコペプチドの質量は理論上のターゲット質量と一致し、質量誤差はわずか 2.14 ppm でした。また、MS/MS データを用いて、特徴的な糖オキソニウムイオン断片を分析し、グリコペプチドの同定を確認しました。図 3B のペプチド配列 (TKPREEQYNSTYR) には、mAb のグリコシル化領域として知られるアスパラギン残基/NXT モチーフが 1 つだけ含まれています。したがって、このグリカンはアスパラギン残基に付加しているものと推論しました。最後に、酵素により mAb からグリカンを分離し、構造をさらに分析しました。この結果も完全版の論文で紹介しています。
感度の高い確実な特性分析
Agilent HPLC-Chip/Q-TOF システムは、商業的な重要性の高いモノクローナル抗体の完全な特性分析を可能にする強力なツールです。貴重なサンプルの消費量をナノグラムレベルに抑えられるこのシステムは、以下のことを可能にします。
この精密で汎用性の高いツールは、細胞株上清のスクリーニングや生産プロセスの最適化、精製から製剤処方まで、開発プロセス全体で mAb の純度や構造の完全性を監視しなければならない診断および製薬関連会社のニーズに応えます。詳細については、LCGC サイトで論文の完全版をご覧ください。