- 製品
- 製品
- CrossLab サポート商品
- サポート商品
- テクニカルサポート
- HOME
- 分野別ソリューション
- ゲノミクス
- 試薬類とキット(ストラタジーン)
- 変異導入
- QuikChange II-E Site-Directed Mutagenesis Kit [RUO]
掲載の製品はすべて試験研究用です。診断目的にご利用いただくことはできません。
正確性の高いエレクトロポレーション
QuikChange II-E Site-Directed Mutagenesis Kit は迅速かつ正確性の高い形質転換が可能なエレクトロポレーション用です。また本製品は、目的以外の変異が導入されないように、PfuUltra DNAポリメラーゼが採用されております。PfuUltra DNAポリメラーゼは、市販のDNAポリメラーゼの中で最高の精確性を誇り、テンプレートを増幅する際に予期せぬ変異導入を最小限に抑えます。この精確性と非PCR法の組み合わせにより、本製品ではランダムな変異導入によるエラーがほとんどありません。
最もフィデリティーの高いDNAポリメラーゼ
QuikChange IIシリーズでは、現在市販されているPCR酵素の中で最もフィデリティー(正確性)の高いPfuUltra high-fidelity DNA polymerase を使用しています。この酵素のエラー率は、平均でPfu DNA Polymeraseの3倍、Taq DNA Polymerase では18倍も低くなっており、これが最も高いフィデリティーを持つ酵素といわれる所以です(表1)。よって特に高いフィデリティーを要する部位特異的変異導入(site-directed mutagenesis)法に有効です。
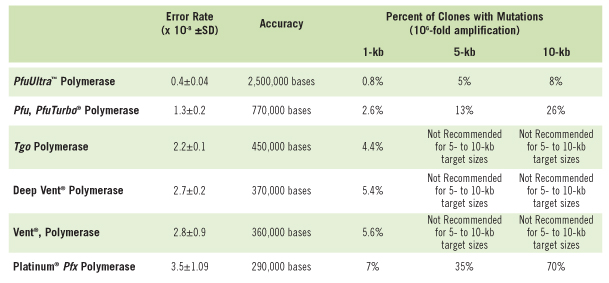
表1 :当社製品PfuUltra high-fidelity DNA polymeraseと市販されている他社製品PCR酵素のエラー率を下記条件にて比較しました。PCR反応溶液50μl中、各プライマー0.2μM 、各ヌクレオチド200μM、プラスミドDNA 25ng、DNAポリメラーゼ2.5U 。例外:Platinum Pfx Polymerase反応溶液50μl中ヌクレオチド300μM、DNAポリメラーゼ1.25U 、伸長反応温度68°C。Tgo Polymerase反応溶液50μl中DNAポリメラーゼ1U 、各プライマー0.4μM、VentR/Deep VentR Polymerase反応溶液50μl中DNAポリメラーゼ1U。
非PCRによる増幅
本製品のプロトコールでは、ミニプレップによるプラスミドDNAや塩化セシウムにより精製したプラスミドDNAがご利用いただけます。このスーパーコイル状の二本鎖DNAプラスミドに加え、目的の変異を導入した同じ領域に相補的にデザインされたプライマーセットが必要となります。これらのプライマーは、PfuUltra DNAポリメラーゼにより、温度サイクルにて伸長され、ニックの入ったプラスミドが形成されます。この後、Dpn I処理により、メチル化されたDNAは特異的に消化されるため、鋳型として用いられた元のプラスミドDNAだけが消化され、変異を含む新たに合成されたプラスミドDNAだけが残ります。ほとんどのE. coli株から単離されるDNAは大腸菌の自己防衛作用としてdamメチル化作用を受けており、これらのメチル化されたDNAはDpn Iの標的となります。次に、目的の変異が導入され、ニックの入ったベクターDNAはXL1-BlueもしくはXL10系のコンピテントセルにトランスフォームされ、クローニングできます。本製品では、少量のテンプレートDNAを、高い精確性のPfuUltra DNAポリメラーゼを用いて、少ないサイクル回数で変異を導入するため、目的の変異導入効率が他の方法に比べとても高く、ランダムなエラーによる目的変異導入以外の変異を最小限に抑えることができます。
原理と実験手順
1. テンプレートの準備 あらかじめ目的の塩基配列を組み込み、ミニプレップ等で精製したプラスミドを用意します。基本的にどのプラスミドでも構いませんが、下記のステップ4でメチル化したアデニンを含む配列を認識し消化する制限酵素のDpn I(5’-GmA▼TC-3’)を用いるため、dam-の大腸菌株(JM110やSCS110)から回収したプラスミドは使用できません。
2. 変異鎖の合成 QuikChange II-E Site-Directed Mutagenesis Kitのメカニズム 通常の3ステップ(denature、annealing、extension)のサイクルで変異鎖を合成します。まず二本鎖鋳型DNAの変性。次に目的の変異を含んだ変異導入プライマーのアニーリング。そしてPfuUltra high-fidelity DNA polymeraseによる伸長反応。通常のPCRによる増幅とは異なり、プライマーの構造上、テンプレートの増幅のみが行われアンプリコン(変異鎖)からの増幅は行われないため、偶発的に発生してしまった目的以外の変異が他の変異鎖に受け継がれることがありません。
3. Dpn Iによる消化 変異鎖の合成が終了した後、Dpn Iによる二本鎖テンプレート(メチル化)およびテンプレート&変異鎖(ヘミメチル化)の消化を行います。これにより、変異鎖だけから成る環状二本鎖が得られますが、この時点では両プライマーの5’末端部にニックが入ったままです。
4. 形質転換 変異を含んだプラスミドを StrataClean Resinで精製。XL1-Blue Electroporation-Competent Cells へトランスフォーメーションし大腸菌内でニックが修復されます。目的の変異を持つ環状二本鎖のベクターが得られます。
| Product | Catalog # | Amount | Price | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||