- 製品
- 製品
- CrossLab サポート商品
- サポート商品
- テクニカルサポート
- HOME
- ライブラリ
- Access Agilent アーカイブ
- アジレントの統合型ソリューションによる、 モノクローナル抗体の N-結合型糖鎖の ハイスループットプロファイリング
治療用モノクローナル抗体 (mAb) のグリコシル化パターンは効能や安全性の面で重要な役割を果たしています。末端ガラクトース (Gal) 残基などの N-結合型糖鎖は、抗体エフェクターの機能に影響を与えるものとして知られています [1]。さらに、高濃度のマンノースの存在は抗体の薬物動態に重大な影響を与える可能性があります [2]。
バイオ医薬品メーカーにとって、グリコシル化パターンの特性解析はバイオ医薬品開発を行う上で重要となっています。バイオシミラーの開発 [3] により、さまざまな発現宿主、製造プロセス、スケール、培養の条件によってグリコシル化のパターンが変化する場合があるため、特性解析の研究はさらに重要なものとなっています。mAb の開発段階、例えばクローン選択中や品質管理などでは、N-結合型糖鎖を抽出し分析するためのハイスループット手法が必要です。
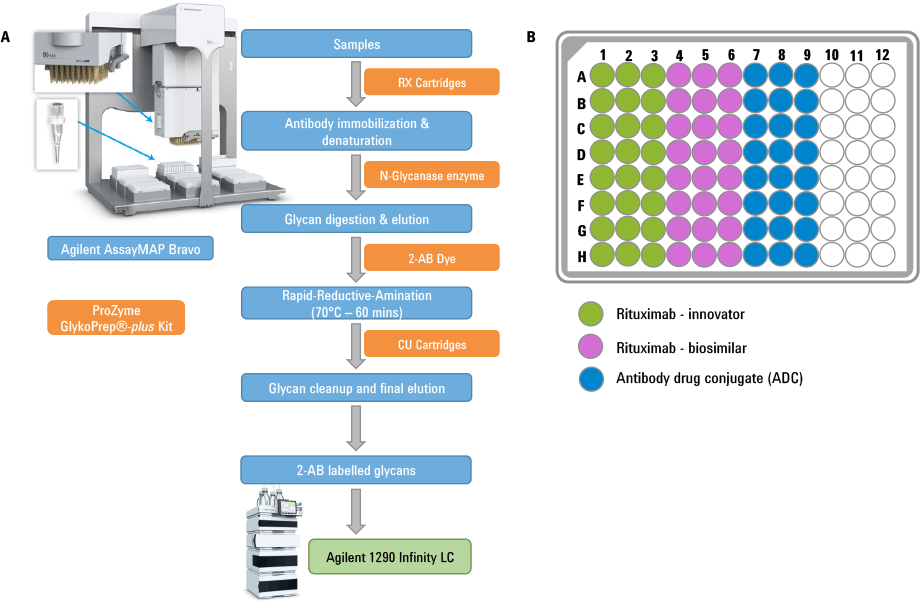
図 1. (A)アジレントのプラットフォームによる LC 分析前の糖鎖単離、ラベリング、精製の概略図。Agilent AssayMAP のステップの内容が青色で、ProZyme キットのステップがオレンジ色で示されています。(B)サンプルロードを示す 96 ウェルプレートのレイアウト。
この記事では、3種類の治療用抗体の N-結合型糖鎖分析におけるサンプル前処理のために Agilent AssayMAP Bravo Platform の適用例をご紹介します。例として、ハイスループット分析をシミュレートするために、96ウェルプレートを使用し、1サンプルあたり 24回の繰り返し分析でサンプル前処理を AssayMAP Bravo にて自動で実行しました。抗体として、リツキシマブ先発品、リツキシマブバイオシミラー、リジン複合化した抗体薬の複合体(ADC)を使用しました。ハイスループット機能は、AssayMAP の小型(5µL)充填マイクロクロマトグラフィーカラムと、精密な液体流量制御機能付き Bravo の 96 チャネルピペットヘッドを組み合わせました。
最初に、ProZyme GlykoPrep plus ラピッド N-結合型糖鎖サンプル前処理と 2-AB キットと AssayMAP N-結合型糖鎖サンプル前処理モジュールを使用して、N-結合型糖鎖の自動サンプル前処理を行いました。図 1 にワークフロー全体の概略図を示します。
次に、VWorks ソフトウェアスイートから N-結合型糖鎖サンプル前処理の RX 消化および 2-AB ラベリングモジュールを使用して、自動化プロトコルを設定しました。
このアプリケーションの詳細については、アプリケーションノート 5991-6904EN と 5991-7024EN をご覧ください。
この分析では、Agilent AdvanceBio Glycan マッピング 300 Å、2.1 x 150 mm、1.8 µm カラムを使用して、精製済み糖鎖の分離を行いました。Agilent AdvanceBio Glycan マッピングカラムは、高速かつ高分離能での再現性のある糖鎖の分離を実現します。これらのカラムは HILIC アミド相互作用を使用し、より適切な分離能と拡散を抑えることで、より高いピークキャパシティを持つことができます。
100 mM ギ酸アンモニウム、pH 4.5 を水層として、アセトニトリルを有機層としてグラジエント溶出で使用し、糖鎖を分離しました。このメソッドを使用し、すべての糖鎖を 6 分以内に分離し、1 サンプルあたりの分析時間を短縮してサンプルスループットを向上しました (図 2)。各サンプルウェルから抽出された糖鎖を 4 回繰り返し分析しました。その結果、Agilent Glycan マッピングカラムは、ピーク高およびピーク面積について 6 % 未満の優れた再現性を示す相対標準偏差 (RSD) を示しました。これにより、Agilent AssayMAP Bravo Platform の再現性の高いサンプル前処理の能力を確認しました。AssayMAP プラットフォームの再現性の詳細については、アプリケーションノート 5991-6904EN を参照してください。
次に、3 種類のサンプルすべてについて各糖鎖種のピーク面積率を計算しました。結果を表 1 に示しました。3 種類のサンプルすべてで主要なグリコ型として G0F N-結合型糖鎖、続いて G1F、G1F’ 異性体、G2F N-結合型糖鎖が同じような傾向の分布を示しました。先発品およびバイオシミラー mAb の糖鎖の面積率についての相関グラフをプロットし、R2 が 0.973 の高い類似性を示しました。
| N-結合型糖鎖 | N-結合型糖鎖の面積率 | |
|---|---|---|
| リツキシマブ 先発品 |
リツキシマブ バイオシミラー |
|
| GO | 1.5 | 0.8 |
| GOF | 42.2 | 50.5 |
| Man5 | 1.7 | 1.2 |
| G1F | 28.6 | 26.7 |
| G1F’ | 13.0 | 11.6 |
| G2 | 0.3 | 0.2 |
| G2F | 8.7 | 5.5 |
| G1FS1 | 0.9 | 0.6 |
| A1F | 0.2 | 0.5 |
| N-結合型糖鎖 | ADC – N-結合型糖鎖の面積率 |
|---|---|
| GO | 4.9 |
| GOF | 43.8 |
| Man5 | 1.3 |
| G1F | 26.8 |
| G1F’ | 13.0 |
| G2F | 6.5 |
| G1FS1 | 0.6 |
表 1. リツキシマブ先発薬、リツキシマブバイオシミラー、抗体薬の複合体の N-結合型糖鎖の面積率。
これらの調査結果は、モノクローナル抗体の N-結合型糖鎖の分析に適したハイスループットワークフローを示しました。ワークフローでは、手作業での操作を減らし高い精度で再現性を高める Agilent AssayMAP Bravo 自動化ソリューションを用いてサンプル前処理を簡素化しました。Agilent AdvanceBio Glycan マッピングカラムにより、高分離能かつ高速な糖鎖分析を実現できました。
Agilent AssayMAP Bravo Platform についての詳細は、このウェブセミナー(注意:音声が再生されます。)でご視聴ください。また、アジレントのカタログで、アジレントの自動化ソリューションにより多忙なラボのスループットおよび効率をどのように高めることができるかをご確認ください。