- 製品
- 製品
- CrossLab サポート商品
- サポート商品
- テクニカルサポート
- HOME
- ライブラリ
- Access Agilent アーカイブ
- 技術のヒント! 水素炎イオン化検出器 (FID) - 検出器情報
はじめに
水素炎イオン化検出器 (FID) は、ガスクロマトグラフィーで用いられる標準的な検出器です。ほぼすべての有機化合物を検出できます。得られるクロマトグラムのピーク面積は、サンプルに含まれる成分の量に相関します。FID はきわめて感度が高く、9 桁という広いダイナミックレンジを備えています。唯一の短所は、サンプル成分が破壊されるという点です。
概略
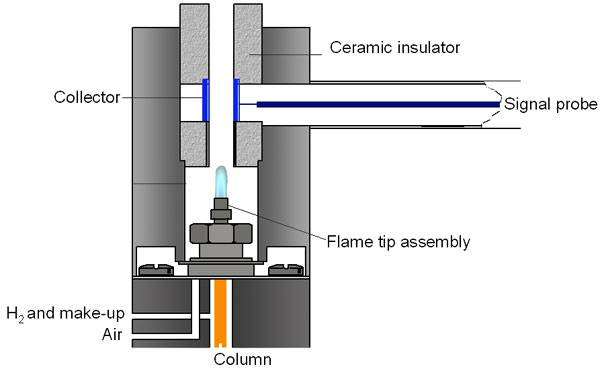
図 1: 水素炎イオン化検出器の概略図
説明
FID は、水素/空気炎とコレクタプレートで構成されます。GC カラムから溶出するサンプルは、炎を通過します。この際、有機分子が分解され、イオンが生成されます。イオンは陽極で回収され、電気シグナルが生じます。コレクタは負の電荷を、炎ジェットは正の電荷をもちます。
メイクアップガスを追加すると、炎の形状が安定します。メイクアップガスとしては、窒素やヘリウムがよく用いられますが、水素が用いられることはありません。最高の感度を得るためには、メイクアップガスの流量を最適化する必要があります (下図参照)。
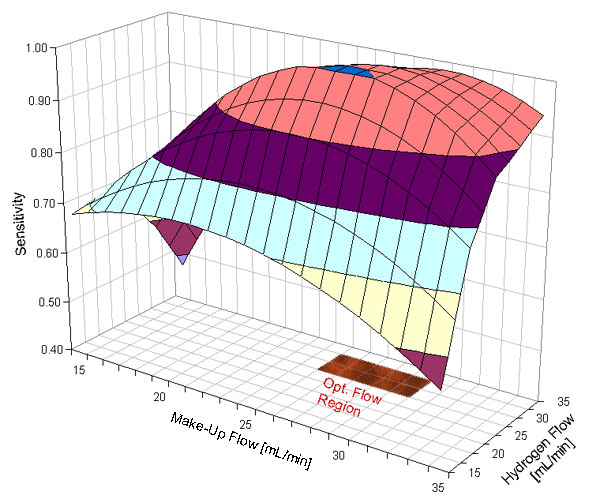
図 2: FID の感度における水素およびメイクアップガス流量の影響
FID における化学反応
オキソメチリウムイオン (CHO+) は、燃焼により生じた周囲の水分子に陽子を奪われ、(オリゴマー) オキソニウムイオン ((H2O)nH+) となります。このイオンが FID で測定されます 。
感度
FID は、濃度に応答する他の多くの検出器とは異なり、流量に応答する検出器です。流量応答または質量応答の場合、検出器ではサンプルの濃度ではなく、マスフローによってレスポンスがあります。また、FID においてn-ヘキサンは n-プロパンの 2 倍のレスポンスになります。
もっと一般的に言えば、FID のレスポンスは、分子中の炭素原子の数に左右されるということです。しかし、すべての炭素原子が、FIDで検出できる形で燃焼するわけではありません。ヘテロ原子が結合している場合や、電子混成が sp3 と異なる場合は、特に検出が難しくなります。
分かりやすい例が、ホルムアルデヒド (H2C=O) です。この化合物では、レスポンスは生じません。
レスポンスがまったくない、またはほとんどない化合物 [8]
FID における一般的な検出下限の仕様は 1-2 pg C•s-1 (1-2 ピコグラムカーボン/秒)、感度の仕様は約15 C•kg-1 (クーロン/キログラム) です。セルボリュームは約 10 nL と無視できる大きさです (イオン化に関わる炎部分のボリューム) [9]。実を言うと、FID はきわめて効率の低いイオン化装置で、成分の 1 ppm しかイオン化されません。しかし、ノイズレベルがきわめて低いため、優れた感度が得られます。
どのくらいのマスフローが測定量または測定濃度に変換されるかはピーク形状と面積によって決まります。ピーク面積は流量が異なっても変化しませんが、ピーク高さは変化します (溶出の早いピークはピーク幅が狭いので、ピーク面積が一定ならピーク高さが高くなります)。
有機化合物のレスポンスを推定するために、Sternberg ら [1] は、有効炭素数 (ECN) というコンセプトを導入しました。これは、ヘテロ原子を含む分子と同じレスポンスを持つn-アルカンとを関連づけるものです。
有効炭素数(ECN)のコンセプト
有効炭素数を用いた方式では、分子に含まれる各原子が付加する寄与が示されます。
ECN 寄与テーブル [2-7]
例
プロパンは、3 つの脂肪族炭素原子で構成されます。したがって、レスポンスは 3 * 1.00 = 3.00 となります。
n-プロパノールは、3 つの脂肪族炭素原子で構成され、第 1 級アルコールです。したがって、レスポンスは 3 * 1.00 - 0.50 = 2.50 となります。
イソプロパノール (第 2 級アルコール) の場合、レスポンスは 3 * 1.00 - 0.75 = 2.25 となります。
3 つの C2-炭化水素 (エタン、エテン、エチン) の場合、レスポンスはそれぞれ 2.00、1.90、2.60 となります。
参考文献
■ アジレント・テクノロジーの 水素炎イオン化検出器のページもご覧ください。
→ 水素炎イオン化検出器 FID の製品ページへ
■ ガスクロマトグラフィーの基礎ページもご覧ください。